Ciri -ciri asid disulfurik dan fungsi bahan ini
- 3461
- 26
- Jeff Glover
Kita semua telah mendengar asid sulfurik, walaupun ia berlalu. Bahan yang sangat menghakis dan berbahaya ini adalah sebatian kimia yang paling dihasilkan di seluruh dunia. Ia amat penting dalam industri minyak, rawatan keluli, pembuatan bahan letupan, detergen dan plastik dan dalam sintesis baja.
Tanpa asid sulfurik, tidak mungkin untuk meningkatkan industri kayu dan kertas, banyak proses kilang tekstil atau pengeluaran bateri. Tidak juga peranan anda dalam industri kimia dilupakan, kerana perlu untuk sintesis asid penting dan sulfat lain untuk proses tertentu.
Dalam erti kata lain, masyarakat tidak akan seperti yang kita ketahui tanpa asid sulfurik, kerana ia memainkan tugas penting dalam industri kimia, di syarikat minyak dan di bidang pertanian, antara banyak perkara lain. Bagaimanapun, tidak semua sebatian sulfur sama -sama dikenali. Di sini kita memberi perhatian kepada yang kurang dikenali untuk penduduk umum: asid disulfurik.
- Artikel Berkaitan: "11 Jenis Reaksi Kimia"
Apakah asid disulfurik?
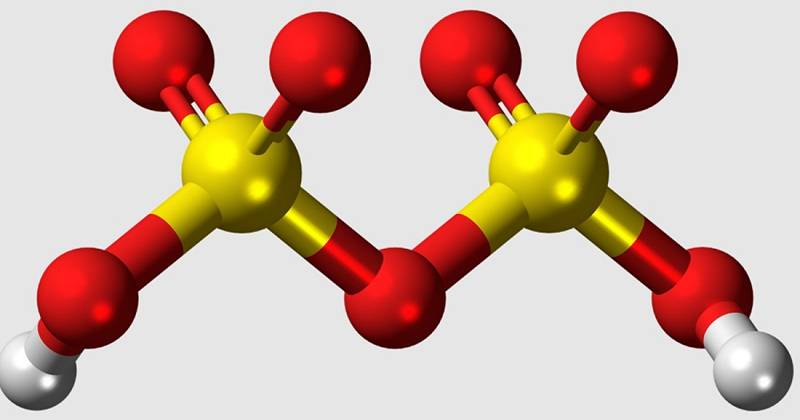
Asid disulfurik, juga dikenali sebagai asid pyrosulfuric atau oleum, adalah oxacid sulfur. Istilah "oxácido" merujuk kepada mana -mana asid yang mengandungi oksigen dalam komposisinya, terutama yang terdapat dalam struktur kimia mereka sekurang -kurangnya satu atom hidrogen (h), salah satu oksigen (O) dan elemen yang berubah -ubah, sama ada x.
Asid disulfurik adalah komponen utama asid sulfurik merokok atau minyak, yang sifat dan kegunaannya akan kita jelaskan di bahagian masa depan. Buat masa ini, kita ditinggalkan dengan kimianya adalah H2SO7. Ini bermakna ia dibentuk oleh dua atom hidrogen (H2), 7 oksigen (O7) dan dua sulfur (S2). Sementara itu, asid sulfurik digunakan, mempunyai dua atom hidrogen, salah satu sulfur dan empat oksigen (H2SO4).
Ia juga menarik untuk menekankan bahawa asid ini mempunyai jisim molar 178.13 g · mol - 1 dan titik leburnya adalah 36 darjah, suhu yang menandakan perubahan pepejal ke keadaan cair. Terdapat asid lain dengan formula yang sama "H2O · (SO3) X", walaupun ini tidak dapat diasingkan dalam keadaan percubaan hari ini.
- Anda mungkin berminat: "15 sifat fizikal dan kimia air"
Ciri -ciri minyak
Seperti yang telah kita katakan, asid disulfurik Ia adalah komponen utama asid sulfurik merokok, juga dikenali sebagai oleum. Formula penyelesaian ini adalah YSO3 · H2O, Sendo "Y" jumlah jisim molar sulfur trioksida (SO3). Bagaimanapun, ia juga boleh ditetapkan dengan tatanama "H2SO4 · XSO3", di mana "X" merujuk kepada kandungan molar sulfur trioksida. Apabila x = 1 e y = 2, formula h2s2o7 diperoleh, atau apa yang sama, asid disulfurik.
Ia mungkin terdengar kompleks, tetapi tinggal dengan idea berikut: Penyelesaian oleum boleh mempunyai sifat yang berbeza mengikut peratusan kepekatan asid sulfurik dan penyesuaian yang disebutkan di atas menimbulkan asid disulfurik, yang berlaku sehingga 36 darjah suhu alam sekitar. Seperti yang menarik bahawa semua konglomerat ini bunyi di bahan kimia, bagaimanapun, adalah perlu untuk menekankan bahawa Asid disulfurik jarang digunakan dalam proses makmal atau perindustrian.
Oleum disintesis oleh "proses hubungan", di mana kumpulan oksigen ditambah kepada sulfur (S+O3, SO3) dan kemudian dibubarkan dalam pekat asid sulfurik (H2SO4). Mungkin bahan kimia akan dibuang dari rambut apabila melihat terlalu banyaknya, tetapi untuk tujuan bermaklumat, kami mengambil lesen untuk menunjukkan kepada anda kesatuan kedua -dua konsep:

Oleh itu, asid oleum atau disulfurik biasa dibina dengan sulfur yang mana oksigen dan menumpukan asid sulfurik telah ditambah. Di dunia kimia, pada akhirnya semuanya juga merupakan soal pengetahuan matematik.
Fungsi dan utiliti bahan ini
Sebaik sahaja kita membedah sifat kimia penyelesaian yang kompleks ini, kita dapat meneroka kegunaannya, walaupun secara ringkas.
1. Pengeluaran asid sulfurik
Walaupun kedengarannya tidak sah, Penyelesaian yang memerlukan asid sulfurik untuk sintesisnya berguna untuk pengeluaran asid sulfurik itu sendiri.
Oleh kerana entalpi penghidratan yang tinggi (perubahan dalam entalpi apabila tahi lalat ion larut dalam air yang mencukupi untuk memberikan larutan yang dicairkan), oleum boleh dicairkan di dalam air untuk menghasilkan asid sulfurik tambahan asid pekat tambahan.
Sebaliknya, jika SO3 ditambah terus ke dalam air, filem asid sulfurik sulfurik yang sangat sukar akan dibentuk.
@Image (28510)
2. Perantara pengangkutan
Oleh kerana oleum dibentangkan dalam keadaan pepejal sehingga 36 darjah suhu, Ia boleh berguna untuk pengangkutan asid sulfurik dalam trak dengan tangki, antara minyak minyak dan pelbagai industri. Sebaik sahaja ia mencapai tujuannya, oleum dapat diubah lagi dalam keadaan cairnya. Bagaimanapun, proses ini mesti dijalankan dengan cara yang sangat berhati -hati, kerana terlalu panas bahan (terlalu panas) melebihi had keselamatan.
Di samping itu, asid oleum atau disulfurik kurang mengakis daripada asid sulfurik untuk digunakan apabila bersentuhan dengan logam, kerana tidak ada molekul air percuma yang dapat menyerang permukaan ini. Oleh itu, kadang -kadang asid disulfurik cecair juga dipilih untuk pengangkutan antara paip kompleks. Oleh kerana keupayaannya untuk "kembali" dalam asid sulfurik pekat dan kemudahannya berubah dari keadaan pepejal menjadi cecair, oleum mempunyai banyak utiliti dalam bidang pengangkutan.
3. Asid disulfurik dalam industri letupan
Oleum juga Ia digunakan dalam sintesis bahan peledak, dengan pengecualian nitrocellulose yang luar biasa. Ini kerana penyelesaian asid nitrik (NO3) dan asid sulfurik (H2SO4, yang boleh diperoleh atau tidak menggunakan asid disulfurik) mengandungi jumlah air yang ketara, sesuatu yang menjadikannya sedikit berguna dalam banyak proses pembuatan bahan peledak.
4. Penggunaan dalam kajian kimia organik
Oleum adalah agen reaktif yang agresif dan sangat menghakis, berguna sebagai perantara dalam tindak balas kimia tertentu.
Ringkasan
Ringkasnya, asid disulfurik dapat dilihat sebagai perantara asid sulfurik, walaupun datang dari reaksi yang memerlukannya pada mulanya. Seperti yang dibentangkan dalam keadaan pepejal secara semulajadi, ditunjukkan untuk pengangkutan yang selamat di banyak sektor industri yang mengendalikan H2SO4 secara semula jadi. Ia juga sangat menarik untuk menggunakan sebatian ini dalam bentuk cecairnya, kerana kurang mengakis daripada asid sulfurik, ia menghasilkan kurang kerosakan pada paip dan lapisan logam lain.
Sekali lagi, kami meneruskan idea bahawa asid sulfurik adalah penting dalam pertanian, kayu, tekstil, minyak dan banyak lagi industri cawangan lain. Oleh itu, walaupun asid disulfurik tidak begitu berguna sebagai sebatian yang terpakai secara langsung dalam bidang makmal, ia memberikan keplastikan tertentu ketika mengangkut, menyempurnakan dan merawat asid sulfurik itu sendiri.

